Es una de las condiciones más frecuentes en la consulta dermatológica y, en medicina estética, constituye un determinante directo de tolerancia, recuperación y satisfacción tras procedimientos. Por ello, la prevención y el manejo precoz de reacciones adversas no deben ser nuestro plan de contingencia, sino parte de nuestro protocolo habitual.
Por la Dra. Cristina Garcia Millán
El síndrome de piel sensible (SSS) es una de las condiciones más frecuentes en la consulta dermatológica, con prevalencias muy variables según la metodología empleada en su registro (especialmente en encuestas de autopercepción), situadas en torno al 40-45 % para la categoría “sensible o muy sensible” y pudiendo alcanzar el 50-70 % cuando se incluyen grados leves de sensibilidad1.
En el entorno de la medicina estética, constituye un determinante directo de tolerancia, recuperación y satisfacción tras procedimientos. Se caracteriza por síntomas subjetivos –escozor, ardor, dolor, prurito u hormigueo– ante estímulos habitualmente inocuos, con piel de aspecto normal o con eritema sin lesiones atribuibles a una patología dermatológica definida¹. La autopercepción de piel sensible se describe con mayor frecuencia en mujeres y se asocia con piel seca, antecedentes de dermatitis atópica y coexistencia de dermatosis inflamatorias (por ejemplo, rosácea), mientras que las diferencias por edad y fototipo no son consistentes entre estudios.
En la práctica, el síndrome de piel sensible actúa como amplificador: a igualdad de técnica, estos pacientes presentan más molestias, eritema más prolongado y mayor riesgo de reactivación de dermatosis de base tras procedimientos. Por ello, la prevención y el manejo precoz de reacciones adversas leves o moderadas deben formar parte del protocolo habitual, no reservarse como plan de contingencia.
Síndrome de piel sensible, dermatosis y dermatitis
La definición consensuada por el grupo de trabajo del International Forum for the Study of Itch (IFSI) describe la piel sensible como un síndrome de sensaciones desagradables en respuesta a estímulos habitualmente inocuos, no atribuibles por sí mismas a lesiones de una enfermedad cutánea, con piel de aspecto normal o con eritema2.
Conviene recordar que esta definición es operativa, pero en la práctica existe un solapamiento clínico y fisiopatológico con entidades como la rosácea eritematotelangiectásica, la dermatitis atópica subclínica y otros cuadros de hipersensibilidad neurosensorial; por ello, en consulta, es más útil identificar desencadenantes y descartar diagnósticos alternativos que basarse únicamente en la etiqueta de SSS.
Pese a su carácter predominantemente subjetivo, el SSS cuenta con instrumentos de evaluación validados (como SS-10, con buen rendimiento diagnóstico) y se ha planteado como un fenotipo de hipersensibilidad neurosensorial relacionado con disfunción de fibras pequeñas, lo que ayuda a explicar la “zona gris” con otros diagnósticos inflamatorios o neuropáticos.
Para la consulta de medicina estética, es útil ordenar los casos en tres escenarios: SSS “primario” (síntomas con semiología mínima), SSS asociado a dermatosis (rosácea, dermatitis atópica, dermatitis seborreica, acné o dermatitis periorificial) y dermatitis de contacto (irritativa o alérgica), que puede confundirse con Síndrome de piel sensible y, con frecuencia, se precipita por cambios en la rutina cosmética periprocedimiento o por exposición a antisépticos y adhesivos.

Fisiopatología útil para el clínico
El SSS es un síndrome, no una entidad etiológica única; sin embargo, la literatura reciente converge en cuatro ejes con valor práctico para el clínico.
El primero es la disfunción de barrera, con mayor pérdida transepidérmica de agua (TEWL) y mayor penetración de irritantes. La barrera epidérmica depende de una proporción equilibrada de ceramidas, colesterol y ácidos grasos libres (3:1:1), cuya alteración es frecuente en SSS y se agrava transitoriamente tras procedimientos ablativos3.
El segundo, la neurosensibilidad cutánea, con umbrales bajos a estímulos químicos, térmicos y mecánicos. Canales TRP (particularmente TRPV1 y TRPA1) se han implicado como mediadores de la hipersensibilidad4.
El tercero, la microinflamación subclínica, con liberación de mediadores proinflamatorios (IL-1α, TNF-α, sustancia P) que perpetúan el ciclo sensibilidad-inflamación- daño de barrera4.
El cuarto, cada vez más documentado, es la alteración del microbioma cutáneo. Algunos tratamientos (peelings, láser CO2, radiofrecuencia) pueden modificar la diversidad microbiana de la piel, ocasionando periodos de recuperación más prolongados en algunos pacientes, que debemos saber identificar5.
Este marco explica dos realidades clínicas: por qué podemos encontrar pacientes que con mínimas agresiones cutáneas padecen síntomas desproporcionados, y por qué la complejidad terapéutica (muchos productos cosméticos pre- y postratamiento, por ejemplo) tiende a empeorar la tolerancia en lugar de mejorarla.
Cribado y estratificación de riesgo
Un cribado eficaz puede realizarse en pocos minutos. En la anamnesis, conviene preguntar por: ardor o escozor con cosméticos (hidratantes, fotoprotectores), mala tolerancia a retinoides o exfoliantes, reactividad marcada a factores climáticos (frío, calor, viento) y antecedentes de recuperaciones postprocedimiento más prolongadas de lo esperable (eritema persistente, prurito, descamación).
En la exploración, los hallazgos que nos ayudan a identificar a los pacientes con mayor riesgo incluyen pieles finas, telangiectasias visibles, rosácea, xerosis, dermatitis seborreica, acné y signos de disrupción de barrera. En AFF, los procedimientos de resurfacing ablativo (por ejemplo, CO2) deben evitarse, especialmente sobre áreas afectadas o en enfermedad activa, por riesgo aumentado de complicaciones cicatriciales y evolución impredecible. Existen cuestionarios validados, como la Sensitive Scale2, que pueden complementar la valoración clínica y contribuir a sistematizar el cribado.
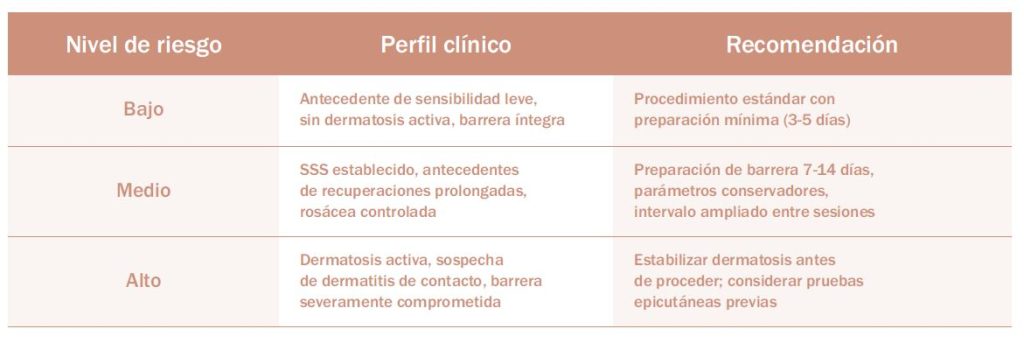
Con esa información, una estratificación sencilla en tres niveles (bajo, medio, alto) ayuda a modular intensidad, intervalos y necesidad de tratamiento dermatológico antes de los procedimientos.
El error clínico típico es intervenir sobre inflamación activa subestimada o falta de reconocimiento de alguna patología previa.
Preparación de barrera
En Síndrome de piel sensible, la prevención debe basarse en la realización del procedimiento con piel estable: barrera funcional, baja inflamación basal y mínima carga de irritantes. Esta “preparación de barrera” suele requerir 7-14 días (más si hay dermatosis activa) y consiste en simplificar la rutina, retirar temporalmente activos irritantes según tolerancia individual (retinoides, AHA/BHA, peróxido de benzoilo, exfoliación mecánica) y reforzar hidratación y fotoprotección.
La retirada de retinoides merece un comentario específico: aunque la práctica habitual es suspenderlos 5-7 días antes de procedimientos ablativos o semiablativos, en algunos protocolos de preparación para peelings medios los retinoides se mantienen para potenciar la penetración. La decisión debe individualizarse según el tipo de procedimiento y la tolerancia previa del paciente.
En cuanto a los emolientes de preparación, los formulados con ceramidas, ácidos grasos esenciales y niacinamida han demostrado eficacia en la restauración de barrera3. La medición de la pérdida transepidérmica de agua (TEWL) puede servir como indicador objetivo del estado de barrera, aunque en la práctica clínica habitual no suele realizarse.
Existe un trabajo de consenso reciente sobre rutina holística en acné, rosácea, dermatitis atópica y Síndrome de piel sensible, que enfatiza limpieza suave, hidratación y fotoprotección como base y herramienta básica de actuación6. En el desarrollo de protocolos médico-estéticos existen además recomendaciones periprocedimiento para estandarizar el antes/durante/después con el objetivo de optimizar la recuperación cutánea y reducir reactividad7. Otro grupo de trabajo enfatiza el enfoque integral para promover la cicatrización, acortar el downtime y optimizar los resultados8.
Un fenómeno que conviene destacar es la superposición de cosméticos , es decir, la aplicación simultánea o muy cercana en el tiempo de múltiples productos y activos tópicos durante el periodo periprocedimiento, que aumenta el riesgo de disrupción de la barrera cutánea. En pacientes con Síndrome de piel sensible, la superposición de cosméticos es una de las causas más frecuentes de persistencia de síntomas y tiempos de recuperación prolongados.
Comunicación con el paciente
En pacientes con Síndrome de piel sensible, la comunicación previa al procedimiento merece atención específica. Estos pacientes presentan con frecuencia una mayor sensibilidad, no solo cutánea, sino también emocional: acumulan frustraciones con tratamientos previos y necesitan una explicación clara de lo que pueden esperar. El consentimiento informado debería incluir: la posibilidad de una recuperación más prolongada, la necesidad de una rutina postprocedimiento simplificada, la importancia de no añadir productos por cuenta propia durante el periodo de recuperación y los signos de alarma que deben motivar consulta anticipada. Dedicar unos minutos a esta comunicación reduce la ansiedad, mejora la adherencia al protocolo tras el procedimiento y disminuye las consultas innecesarias.
Reacciones adversas frecuentes
En pacientes con Síndrome de piel sensible, la mayoría de reacciones adversas son de carácter inflamatorio y funcional. El objetivo inicial es distinguir la respuesta esperable de la patológica, interrumpir el factor perpetuador y evitar la cronificación.
➤ Eritema persistente. Tras procedimientos con energía (radiofrecuencia, láser fraccionado, CO2 fraccionado), un grado de eritema y molestias iniciales puede ser esperable; pero, cuando se prolonga más allá del tiempo previsto para el procedimiento realizado o progresa en intensidad, deben considerarse irritación por barrera comprometida, reactivación de rosácea y dermatitis de contacto por antisépticos o cosméticos postprocedimiento. En resurfacing con CO2 fraccionado, la dermatitis de contacto posoperatoria es una entidad relevante, potencialmente difícil de distinguir del eritema postratamiento si el paciente aplica múltiples tópicos sobre una barrera alterada: la retirada precoz del agente sospechoso y el soporte de barrera son claves9.
➤ Descamación y prurito. En Síndrome de piel sensible, estos síntomas suelen mejorar con la reducción de estímulos y una rutina mínima. Es frecuente que el paciente “compense” la sensación con más productos, incluyendo calmantes perfumados o con múltiples extractos; esto incrementa el riesgo de dermatitis irritativa o alérgica. En este escenario suele ser más eficaz simplificar que añadir. El emoliente ideal en esta fase es un producto con mínimos componentes, sin fragancia y con función de restauración de barrera (ceramidas, pantenol o niacinamida).
➤ Reactivación de dermatosis subyacentes. Rosácea, dermatitis seborreica y dermatitis periorificial pueden reactivarse con inflamación, calor local, fricción y cambios bruscos de rutina. La prevención pasa por tratar la actividad basal antes del procedimiento, espaciar sesiones y ajustar parámetros.
➤ Papel emergente del microbioma en la recuperación postprocedimiento. Los procedimientos que implican disrupción de barrera –particularmente los ablativos– alteran transitoriamente la composición del microbioma cutáneo, reduciendo la diversidad microbiana y favoreciendo potencialmente el sobrecrecimiento de patógenos oportunistas5. Aunque la evidencia es aún preliminar, algunos autores han propuesto la incorporación de posbióticos tópicos en el periodo de recuperación como estrategia para restaurar el equilibrio microbiano y acelerar la reparación de barrera10. Este es un campo en evolución que merece seguimiento.
➤ Dermatitis perioral/periorificial postprocedimiento y por superposición de cosméticos. La dermatitis periorificial es especialmente relevante en medicina estética porque puede presentarse como un postprocedimiento “difícil”, con ardor, eritema y pápulas/pústulas periorales, perinasales y/o perioculares. Una revisión reciente en The Journal of the American Academy of Dermatology (JAAD) resume la fisiopatología (factores incitantes, disfunción de barrera, inflamación y microbioma) y propone un enfoque diagnóstico-terapéutico escalonado11.
En cuanto a la relación con procedimientos, un estudio en Journal of Cosmetic Dermatology comparó radiofrecuencia con microagujas sola frente a su combinación con láser de tulio (1927 nm), reportando entre los eventos adversos la aparición de dermatitis perioral, lo que refuerza la plausibilidad de que la agresión y la inflamación local precipiten el cuadro en pacientes susceptibles12.
La relación con cosméticos y oclusión está apoyada por estudios clásicos: Malik y Quirk describieron asociaciones entre aplicaciones tópicas y dermatitis perioral13, y Dirschka et al. encontraron relación con uso de cosméticos en un estudio basado en cuestionarios14. Datos de StatPearls indican que la aplicación superpuesta de base de maquillaje sobre humectante y crema nocturna multiplica por 13 el riesgo de dermatitis perioral, un dato con implicación directa para el consejo postprocedimiento15.

Reconocer la dermatitis de contacto
Debe sospecharse dermatitis de contacto cuando predomina el prurito, existe eccema claro, hay patrón compatible (periocular, perioral o en zonas de aplicación) o el paciente empeora con productos de uso habitual. En ocasiones, la clorhexidina y otros antisépticos pueden producir reacciones retardadas o inmediatas; una revisión en Plastic and Reconstructive Surgery- Global Open resume el reconocimiento y manejo de complicaciones alérgicas perioperatorias, cuyo enfoque es trasladable al contexto de la consulta de medicina estética16.
Ante dermatitis recurrente o persistente, o cuando la sospecha de alergia condiciona procedimientos futuros, debe considerarse la indicación de pruebas epicutáneas. La serie estándar del GEIDAC permite identificar los alérgenos de contacto más prevalentes en nuestro medio; en pacientes con exposición específica a cosméticos, puede complementarse con la serie de cosméticos y fragancias17.
En la práctica, esto se traduce en un mensaje preventivo claro: evitar la superposición de cosméticos tras el procedimiento, especialmente cuando la barrera está transitoriamente alterada.
El manejo inicial en sospecha de dermatitis periorificial postprocedimiento debe seguir un enfoque escalonado:
- Retirada de corticoides tópicos faciales si se están usando (con retirada guiada si hay dependencia).
- Instaurar una rutina mínima de recuperación de barrera durante 2-4 semanas: limpiador suave, emoliente sin fragancia y fotoprotector mineral.
- Considerar antibioterapia oral (doxiciclina a dosis antiinflamatoria, 40-50 mg/día) y tratamiento tópico (ivermectina, metronidazol, inhibidores de calcineurina según el caso).
- Evitar exceso de producto tópico en fases iniciales, pues suele empeorar el cuadro. La tentación de “tratar más” es el principal error de manejo en esta entidad.
Integrarlo en el protocolo
El SSS no es una contraindicación para procedimientos estéticos, pero sí una condición que exige protocolo. Su reconocimiento, un cribado breve, preservar la función barrera (frágil en estos pacientes), la aplicación de parámetros prudentes y un plan periprocedimiento sencillo reducen las reacciones adversas y mejoran los resultados.
En el manejo, la clave es identificar patrones, evitar la superposición de cosméticos y distinguir Síndrome de piel sensible de otras entidades, sin olvidar la dermatitis de contacto, que en ocasiones puede ser difícil de reconocer. Por último tener en cuenta la dermatitis periorificial como complicación posible tras dispositivos basados en energía o tras cambios en la rutina cosmética permite intervenir precozmente y evitar la cronificación. En un entorno en el que la demanda de procedimientos estéticos crece entre pacientes con piel sensible, integrar el SSS en el protocolo de consulta constituye un elemento diferencial.

Dra. Cristina García Millán
Dermatóloga
La Dra. García Millán inició su actividad en el campo de la dermatología en el año 2004, especializándose en piel sensible, dermatología estética y pedriátrica y tratamiento láser. Actualmente dirige Esthea Medica (Madrid), clínica de la que es fundadora. Con anterioridad, desarrolló su labor asistencial en el Hospital Universitario Ramón y Cajal, en el Hospital Universitario Sanitas La Moraleja y en el Grupo Dermatológico Pedro Jaén, donde fue responsable de la Escuela de Dermatitis Atópica y Piel Sensible y la Unidad de Dermatología Pediátrica. Complementa su actividad profesional con la labor docente, siendo profesora en diversos másters y cursos de la Universidad Alcalá de Henares. Es miembro de diversas sociedades médicas y científicas, publica periódicamente y participa con regularidad en simposios, reuniones y congresos de dermatología. Además de su labor asistencial, colabora como consultora con la industria farmacéutica y cosmética, donde asesora en el ámbito científico, formativo y de práctica asistencial.
Puedes consultar aquí toda la bibliografía









Deja una respuesta