Evidencia actual y recomendaciones
En el presente artículo revisamos los fundamentos biológicos, justificación científica y cronología de las terapias físicas que usan luz (de baja o alta intensidad) como herramientas útiles y seguras para afrontar las secuelas estéticas de los pacientes oncológicos, siempre y cuando se utilicen bajo los criterios médicos necesarios.
Por la Dra. Paloma Sosa Fajardo
La cronificación del cáncer y el aumento de la supervivencia de los pacientes ha transformado profundamente la oncología, desplazando el foco de manera exclusiva en la curación hacia un enfoque más integral que contemple no solo la respuesta tumoral sino también la restauración funcional y cosmética de las secuelas. En este contexto, la medicina estética se perfila como una herramienta fundamental para la correcta recuperación funcional y la mejora de la calidad de vida. Los tratamientos fundamentados en terapias de luz permiten actuar sobre la piel, el tejido subcutáneo y las estructuras afectadas por cirugía, quimioterapia o radioterapia. Sin embargo, su uso requiere criterios estrictos de seguridad, conocimiento del historial médico y coordinación multidisciplinar.
El presente artículo responde a tres preguntas esenciales: cómo, cuándo y por qué aplicar terapias de luz con fines estéticos en pacientes oncológicos, apoyándose en la evidencia científica y la experiencia clínica de los últimos años.
Evaluación y seguridad
El primer paso en la atención estética del paciente oncológico es la valoración médica integral. Es imprescindible conocer:
- Tipo de neoplasia y tratamientos recibidos
- Tiempo transcurrido desde la última terapia oncológica
- Presencia de fibrosis, linfedema o alteraciones vasculares
- Estado inmunológico y condición cutánea
La comunicación con el oncólogo radioterápico o médico responsable es clave para descartar contraindicaciones y coordinar la intervención estética.
Fotobiomodulación (LLLT)
Basada en la emisión de luz de baja intensidad, conocida en inglés como low-level laser therapy (LLLT) o light-emitting diodes (LED) (660-904 nm), la fotobiomodulación (FBM) promueve la regeneración celular, reduce la inflamación y acelera la cicatrización1.
La FBM actúa a nivel celular estimulando la producción de ATP a través de la mitocondria, concretamente mediante la citocromo c oxidasa (fig.1). Se produce un aumento de concentración de ATP intracelular y se generan grandes cantidades de radicales libres del oxígeno, que a su vez activan la vía canónica del TGF-B (la vía de las SMADs). Todo este proceso culmina en la activación de genes de proliferación celular, regeneración y producción de colágeno.
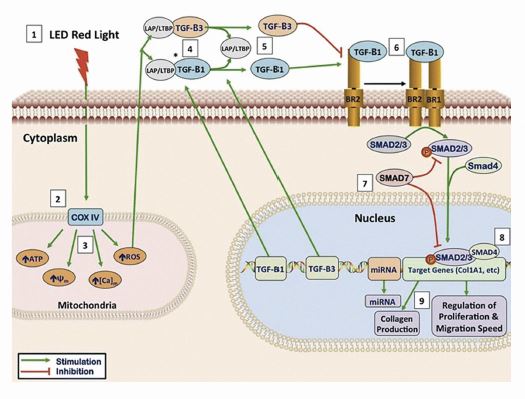
Fig. 1. Cascadas intracelulares activadas por las técnicas de luz de baja intensidad (fotobiomodulación). Se observa, entre otras, la producción de ATP y el aumento de radicales libres del oxígeno, que a su vez atraen y activan la vía de las SMADs a través del TGF-B. Fuente: https://piel-l.org/blog/43703.
Consideraciones importantes
Sin embargo, la activación de cascadas de proliferación celular y aumento de la velocidad de migración podrían suponer en células tumorales un estímulo protumoral de regeneración celular. Estudios como el de Hamblin en 20181 demostraron que este estímulo tumoral no ocurría debido a la manera de obtener energía que tienen las células tumorales.
Mientras las mitocondrias sanas realizan la fosforilación oxidativa (proceso del que obtienen 36 moléculas de ATP por cada molécula de glucosa), las mitocondrias tumorales sufren el conocido efecto Warburg (fig.2). Este efecto consiste en la predilección de las células tumorales de obtener energía mediante la glicólisis en lugar de la fosforilación oxidativa, a pesar de que se encuentren en situaciones de normoxia2.
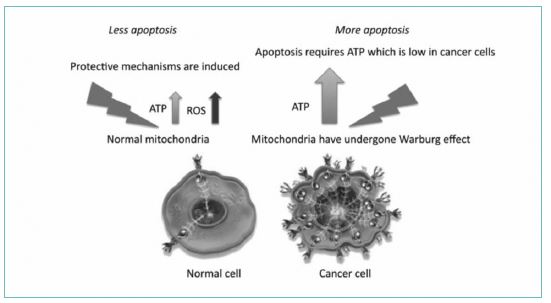
Fig. 2. Gráfica que muestra la diferencia de obtención de energía de una célula sana vs. célula tumoral cuando se la estimula mediante FBM.
La glicólisis anaerobia es un método subóptimo de obtención de energía en ausencia de oxígeno, al que los tejidos normales recurren en situaciones de hipoxia como el ejercicio físico. Por cada molécula de glucosa solo se producen dos moléculas de ATP, generándose además muchos metabolitos intermediarios como el piruvato y el lactato. La célula tumoral busca deliberadamente realizar la glicólisis aerobia debido a que esos metabolitos intermedios son necesarios para que el tumor pueda continuar sintetizando nuevas células, así que decide sacrificar la optimización energética en pro de aumentar la concentración de estos metabolitos (fig.3).
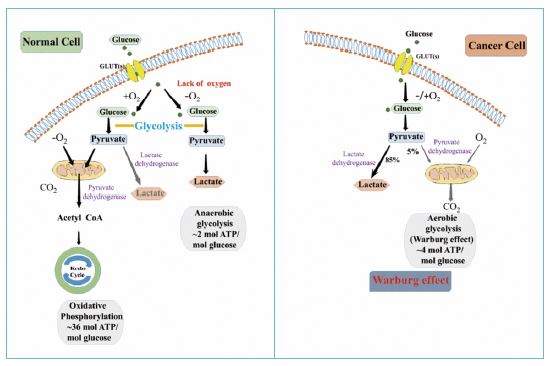
Fig. 3. Cascadas intracelulares de la fosforilación oxidativa (a la izquierda); glicólisis anaerobia (en el centro) y glicólisis aerobia/efecto Warburg (a la derecha)2
El efecto Warburg es el que impide que la FBM tenga un efecto protumoral en estos tejidos, ya que, aunque estemos recibiendo un estímulo para aumentar la síntesis de ATP, la célula tumoral no es capaz de sintetizarlo en más cantidad a través de la glicólisis aerobia.
La FBM se postula como un método oncológicamente seguro para combatir los efectos adversos derivados de los tratamientos oncológicos. La mayor evidencia se acumula en cáncer de mama y cáncer de cabeza y cuello, siendo sus beneficios más estudiados en radiodermitis, mucositis, linfedema, fibrosis y dolor3-7. Esta terapia acelera la cicatrización de heridas, disminuye la inflamación, previene la fibrosis, disminuye el dolor y mejora la funcionalidad.
Cáncer de mama
En una revisión reciente7 se detectaron 9 estudios que evaluaban el papel de la fotobiomodulación en el manejo de la toxicidad de la radioterapia en el cáncer de mama. Dos de los estudios aleatorizados más relevantes, por ser actuales y contar con un buen tamaño muestral (120 y 70 pacientes, respectivamente), fueron los de Robijns et al y Strouthos et al; que estudiaron la fotobiomodulación a través de la terapia láser MLS (Multiwave Locked System) o mediante un diodo emisor de luz (LED; THOR Photomedicine Ltd). Ambos demostraron mejoría de la descamación húmeda.
En ambos estudios se administraba tratamiento láser 2 días en semana inmediatamente después o inmediatamente antes de la RT, respectivamente, empezando el día del inicio de esta. El grupo de Robijns demostró que el porcentaje de pacientes que desarrollaba radiodermitis G>2 era superior en el brazo placebo (30 % vs. 6,7 %; p=0,004). Similares resultados obtuvo el grupo de Strouthos, en el que la radiodermitis G>2 y el dolor intenso fueron más frecuentes en el brazo placebo que en el de tratamiento con fotobiomodulación (radiodermitis G2 40 % vs. 12 % y dolor VAS 26,7 % vs. 0 %, respectivamente).
Linfedema
Dos metaanálisis5,8 demostraron también su beneficio en el linfedema, aplicando FBM una media de 3 veces en semana durante el tratamiento con radioterapia en unos 10-17 puntos en la axila irradiada, separados entre ellos por unos 2 cm, con 904 nm en varios de los estudios. El brazo de pacientes que recibió FBM tuvo menos linfedema y menos dolor que el brazo control.
Mucositis
En mucositis, el estudio de Silva et al9 randomizó a 30 pacientes que se encontraban en tratamiento activo con quimioterapia a recibir LLLT (15 pacientes en el brazo experimental) frente a no recibirlo (15 pacientes en el brazo control). Se realizaron sesiones diarias en 10 puntos repartidos por toda la mucosa de la cavidad oral, aplicando una energía de 660 nm de longitud de onda y permaneciendo 4 segundos en cada punto. El brazo de tratamiento desarrolló mucositis menos intensa, de aparición más tardía y menos prolongada en el tiempo que el brazo control (fig.4).
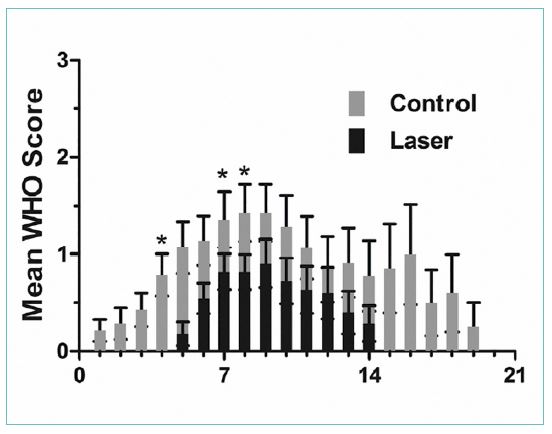
Fig. 4. Evaluación clínica de la severidad de la mucositis inducida por quimioterapia en pacientes con tumores hematológicos desde el día de la administración del ciclo hasta 21 días después. La información se muestra como mediana y desviación estándar de la media. Los asteriscos (*) representan diferencias estadísticamente significativas entre el grupo control y el láser (p<0,05) con respecto a la severidad de la mucositis oral en los días +4, +7 y +8.
Cavidad oral. El grupo de López-Espinoza et al 10está trabajando en desarrollar un protocolo de tratamiento sistemático de toda la cavidad oral (fig.5) utilizando LLLT con unas longitudes de onda de 660 nm (roja) y 808 nm (infrarroja) en 20 puntos de la cavidad oral, 20 segundos por punto, 2 J por punto.
Por tanto, la terapia de FBM parece representar un recurso seguro para combatir los efectos secundarios de los tratamientos oncológicos.
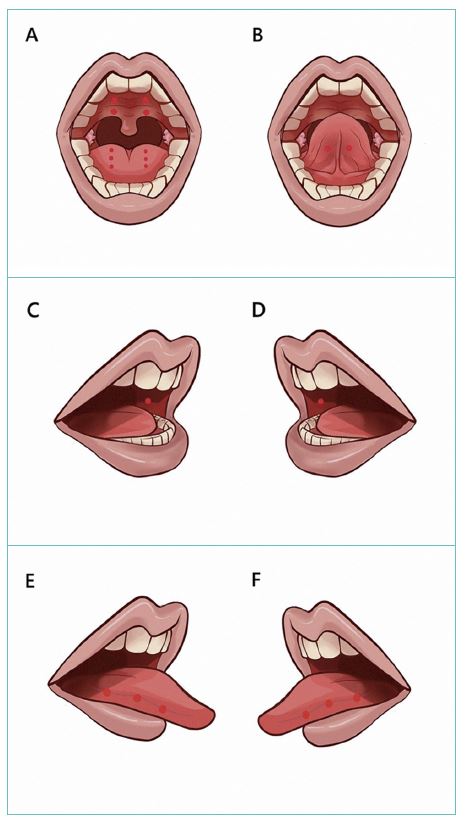
Fig. 5. Distribución de las zonas a tratar de la mucosa oral en base al protocolo en estudio.
Láser e IPL
Los sistemas de luz intensa pulsada (IPL) y láser utilizan luz de alta intensidad. La principal diferencia entre ambos dispositivos es que el láser aplica una luz selectiva y monocromática sobre una superficie puntual y la terapia mediante IPL genera una luz policromática y de amplio espectro que puede incidir sobre múltiples cromóforos y en una superficie más amplia de manera simultánea.
Preguntas y consideraciones
① ¿Pueden estas terapias llegar a inducir cáncer sobre la piel sana?
La respuesta en base a la literatura disponible hasta la fecha es que no hay evidencia que relacione estas terapias con la inducción de tumores cutáneos11,12. Tanto los dispositivos láser como IPL utilizan radiaciones no ionizantes, por lo que no tendrían capacidad de inducir lesiones en el ADN. Las roturas de cadena simple o de doble cadena del ADN inducidas habitualmente por la radiación ionizante son las que, en caso de no ser reparadas adecuadamente, pueden generar mutaciones que se acumulen en el ADN celular y eventualmente acaben favoreciendo la carcinogénesis.
La única radiación no ionizante asociada con la carcinogénesis es la radiación ultravioleta (UV), que habitualmente ocurre por debajo de los 400 nm. Tanto la terapia láser como el IPL trabajan por encima de estas longitudes de onda, razón por lo que se consideran terapias seguras.
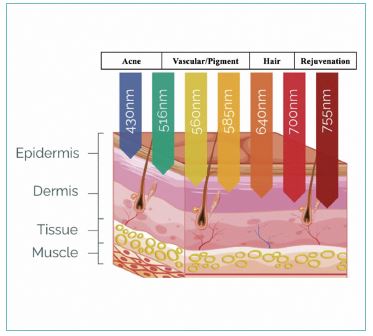
Fig. 6. Distintas longitudes de onda de las terapias de luz con sus correspondientes patologías tratadas.
En un estudio realizado en ratones13 que intentaba discriminar la existencia de un posible poder carcinogénico
de la terapia IPL se expuso a los ratones a luz UV y a terapia IPL, demostrando que el potencial carcinogénico únicamente dependía de la exposición UV, independientementede que los ratones hubiesen sido expuestos o
no a terapia IPL.
② ¿Pueden estas terapias inducir cáncer sobre una piel con lesiones premalignas?
La principal lesión premaligna cutánea es la queratosis actínica (QA). Las QA son lesiones pequeñas, coloreadas e irregulares que aparecen típicamente en zonas fotoexpuestas. Se conoce que en torno a un 5-10 % de las QA pueden ser precursoras de tumores cutáneos, concretamente de carcinomas espinocelulares. Es importante tener en cuenta que una QA nunca será una lesión precursora de un melanoma12.
Varios son los estudios que han demostrado el beneficio del tratamiento de las QA con terapias de luz en combinación con una sustancia fotosensibilizante, frecuentemente ácido 5 aminolevulínco (ALA). Hasta un 68 % de las QA pueden desaparecer tras la primera sesión de ALA-IPL, aunque se recomienda no aplicar solo una sesión, ya que en los estudios en los que se realizaron biopsias cutáneas confirmatorias ocasionalmente se detectaron restos celulares viables a pesar de la desaparición clínica de la lesión14,15.
Con respecto al tratamiento con láser, también existen estudios de eliminación de lesiones pretumorales mediante técnica de resurfacing. En el estudio elaborado por Massey et al16, dos pacientes con múltiples lesiones actínicas y fotoenvejecimiento facial se sometieron a un tratamiento de resurfacing mediante láser CO2. Durante el seguimiento de 52 meses no desarrollaron ninguna lesión tumoral en la zona tratada, desarrollándolas sin embargo en la piel no tratada con terapia láser.
③ ¿Pueden estas terapias generar una progresión tumoral sobre un tumor ya establecido?
Este probablemente sea el aspecto que más atención requiera, ya que las terapias de luz no deben ser utilizadas como tratamiento de lesiones malignas ya establecidas. En este contexto cobra especial relevancia la valoración dermatológica. Antes de realizar tratamientos con terapias de luz sobre lesiones que sugieran un diagnóstico diferencial con una tumoración cutánea el paciente debería ser valorado por un dermatólogo.
Hay series de casos recogidas, como la de Zipser et al en 201017, en la que se describe cómo 12 pacientes diagnosticados de forma tardía de melanoma habían recibido con anterioridad tratamiento con una terapia de luz para lesiones focales que en ese momento se habían diagnosticado como lesiones benignas. No hay manera retrospectiva de dilucidar si las lesiones tratadas con láser eran realmente melanomas, ya que carecían de biopsia, así que la prudencia debería reinar siempre en estas situaciones.
④ ¿Se pueden aplicar en pacientes que estén recibiendo tratamiento oncológico activo?
Muchos tratamientos oncológicos (radioterapia, quimioterapia, terapias sistémicas) pueden inducir fotosensibilidad o incluso fototoxicidad.
En un paciente que haya recibido un tratamiento de esta índole es crucial realizar un enfoque multidisciplinar y coordinado con su oncólogo radioterápico o médico de referencia. En estos casos siempre se debería priorizar el tratamiento oncológico por encima del estético, y se deben evitar a toda costa actuaciones estéticas que comprometan el correcto devenir de los tratamientos antineoplásicos.
El momento adecuado para introducir aparatología depende del tipo de tratamiento oncológico, la localización y el estado clínico del paciente, por lo que siempre será una decisión consensuada con su oncólogo de referencia, pero, a título orientativo, se deberían respetar determinados tiempos (fig.7).
El seguimiento conjunto entre oncólogo, dermatólogo y médico estético permite identificar el momento idóneo y minimizar riesgos de inflamación, necrosis o hiperpigmentación postinflamatoria.
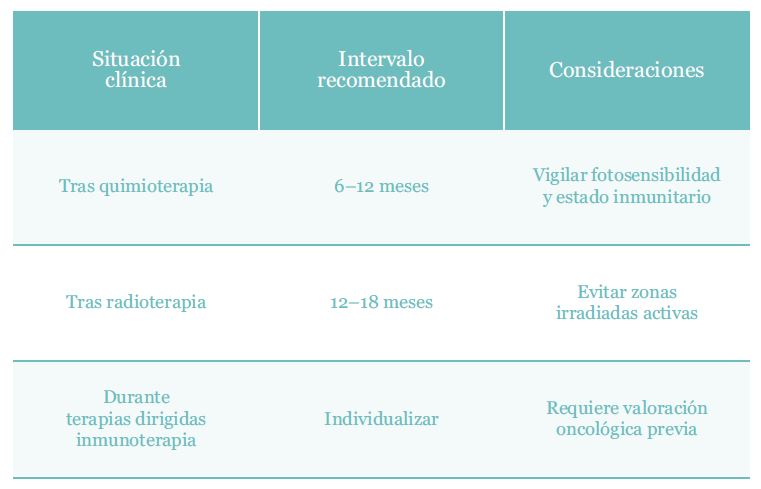
Fig. 7. Cronograma orientativo para reintroducción de aparatología estética según tratamiento oncológico
Beneficios clínicos y psicosociales
Las secuelas estéticas del cáncer afectan profundamente la autoestima, la percepción corporal y la reintegración social.
La aparatología estética, correctamente indicada, ofrece beneficios tangibles:
- Reducción de fibrosis y dolor
- Mejora de la vascularización y del drenaje linfático
- Recuperación de la elasticidad y función muscular
- Aumento de autoestima y bienestar emocional
- Tratamiento de cicatrices
Estas intervenciones se integran en el concepto de supervivencia oncológica activa, donde la estética médica complementa la rehabilitación funcional y psicológica.
Conclusiones
El uso de terapias de luz con fines estéticos en pacientes oncológicos es seguro y eficaz cuando se realiza bajo supervisión médica y con conocimiento del contexto clínico.
El éxito depende de una planificación individualizada, del uso de parámetros validados y de la colaboración multidisciplinar entre oncología, medicina estética, fisioterapia y dermatología.
El futuro de esta disciplina exige protocolos basados en evidencia, formación específica y comunicación continua entre profesionales para que la medicina estética se consolide como herramienta terapéutica en la recuperación integral del paciente oncológico.

Dra. Paloma Sosa Fajardo
Doctora especialista en medicina estética.
Licenciatura en Medicina y Cirugía por la Universidad de Sevilla. Especialista en Oncología Radioterápica en el Complejo Hospitalario Universitario de Santiago de Compostela.
Máster en Medicina Estética por la Universidad Complutense de Madrid.
Profesora asociada del Máster en Oncología Radioterápica (Univ. CEU Cardenal Herrera).
Profesora asociada del Curso OPE Oncología Radioterápica y de los de Experto Universitario en SRS/SBRT y en Delineación Volumétrica para Técnicas Avanzadas de Radioterapia (Univ. Francisco de Vitoria).
Miembro de la junta directiva del Grupo de Oncología para el Estudio del Cáncer de Pulmón (SEOR) y miembro de SOG, SAC, SEME.
Oncóloga radioterápica en Hospital Universitario Virgen del Rocío, Sevilla. Especialista en cáncer de pulmón, técnicas estereotáxicas y cáncer de mama.
Médico estético en Clínicas Lemon (Sevilla, Huelva y Málaga) y Clínica Velázquez (Sevilla).
Bibliografía
- Hamblin MR, et al. Photomed Laser Surg. 2018;36(5):241–5. http://dx.doi.org/10.1089/pho.2017.4401
- Eslami V, et al. J Gastrointest Cancer. 2020;51(3):963–972.
- Zecha JAEM, et al. Support Care Cancer. 2016;24(6):2781–92. http://dx.doi.org/10.1007/s00520-016-3152-z
- Carvalho HA, et al. Oral Oncol. 2011;47(5):431–435.
- Smoot B, et al. J Cancer Surviv. 2015;9(3):405–415.
- Ramos Rocha S, et al. J Lasers Med Sci. 2022;13:e42. http://dx.doi.org/10.34172/jlms.2022.42
- Robijns J, et al. Photobiomodulation, Photomedicine, and Laser Surgery. 2020;38(6):332–9. doi: 10.1089/photob.2019.4761.
- Chiu S-T, et al. Lasers Med Sci. 2023;39(1):11. http://dx.doi.org/10.1007/s10103-023-03959-z.
- Silva AP, et al. Lasers Med Sci. 2014;29(2):645–652.
- López-Espinoza T, et al. BMJ Open. 2024;14(10):e088073. http://dx.doi.org/10.1136/bmjopen-2024-088073
- Gold MH, et al. J Cosmet Dermatol. 2024;23(2):347–354. Ash C, et al. Lasers Med Sci. 2017;32(8):1927–33.
- Hedelund L, et al. Lasers Med Sci. 2006;21(4):198–201. http://dx.doi.org/10.1007/s10103-006-0395-9.
- Kim HS, et al. Dermatol Surg. 2005;31(1):33–6; discussion 36-7. http://dx.doi.org/10.1111/j.1524-4725.2005.31003
- Bhattacharya P, et al. Biomed Mater. 2023;18(4):045005.
- Massey RA, et al. Dermatol Surg. 1999;25(6):513–6. http://dx.doi.org/10.1046/j.1524-4725.1999.08260.x
- Zipser MC, et al. Eur J Dermatol. 2010;20(3):334–8. http://dx.doi.org/10.1684/ejd.2010.0933











Deja una respuesta